amorphe Festkörper

Hans-Peter Ahlsen
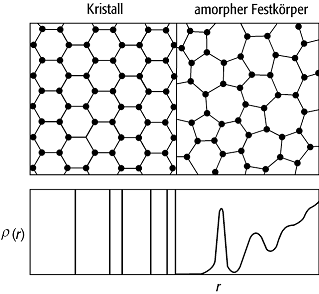
ein Stoff im festen Aggregatzustand ohne periodische Anordnung der Atome in einem Gitter. Beugungsexperimente von Röntgen-, Neutronen- oder Elektronenstrahlen an amorphen Festkörpern liefern aufgrund der fehlenden Fernordnung keine scharfen Reflexe wie bei Kristallen, jedoch existiert eine Nahordnung, die zu verbreiterten Beugungsmaxima führt. Die radiale Verteilungsfunktion r(r), die die Wahrscheinlichkeit dafür angibt, dass im Abstand r von einem Atom ein weiteres gefunden wird, hat für Kristalle und amorphe Festkörper jeweils einen unterschiedlichen Verlauf (Abb.). Amorphe Festkörper zeigen keine Anisotropie, da durch das Fehlen von Kristallachsen keine Richtung ausgezeichnet ist. Jedoch ist die Verteilung der Atome im Nahordnungsbereich eines herausgegriffenen Atoms schon wegen ihrer endlichen Grösse nicht in allen Richtungen gleich, man spricht von einer statistischen Isotropie. Zwischen dem amorphen Zustand und dem idealen Kristall sind die Flüssigkristalle und die parakristallinen Substanzen einzuordnen. In der Praxis ist die Struktur amorpher Materialien oft nicht vollständig homogen, sondern man hat kristalline Ausscheidungen, deren Volumenanteil jedoch unterhalb der Nachweisgrenze z.B. von Experimenten zur Röntgenbeugung liegt. Solche Materialien bezeichnet man als röntgenamorph. Bekannte Beispiele für amorphe Festkörper sind Harze und Oxide auf Silikatbasis wie SiO2, die zu den Gläsern zählen. Man kennt auch eine Reihe von metallischen Gläsern. Technische Anwendungen finden insbesondere amorphe Halbleiter und amorphe magnetische Materialien.
Strukturelle Einflüsse auf physikalische Eigenschaften machen sich besonders bei tiefen Temperaturen bemerkbar, so dass nahe dem absoluten Nullpunkt systematische Abweichungen der Eigenschaften eines amorphen Festkörpers von denen des Kristalls zu verzeichnen sind. Amorphe Substanzen haben eine höhere spezifische Wärmekapazität c und eine geringere Wärmeleitfähigkeit k. Auch die Temperaturabhängigkeiten nahe T = 0 sind mit c ~ T, k ~ T2 charakteristisch für amorphe Substanzen, während im Kristall c und k proportional zu T3 sind (Debyesches T3-Gesetz). Eine Erklärung hierfür liefern einfache Modellvorstellungen, nach denen die Atome in amorphen Substanzen zwei mögliche Gleichgewichtslagen haben, die durch eine Potentialbarriere voneinander getrennt sind, so dass bei T = 0 nur die energetisch niedrigsten Zustände besetzt sind. Eine Temperaturerhöhung bewirkt eine Teilbesetzung der höheren Zustände, wodurch sich für die spezifische Wärme c ~ T ergibt.
In amorphen Metallen und Legierungen ist der elektrische Widerstand wesentlich höher als im Kristall und hängt nur wenig von der Temperatur ab. Eine anschauliche Erklärung ist die Vorstellung, dass in der ungeordneten Struktur alle Atome Gitterfehler darstellen, welche in Kristallen eine Abweichung vom periodischen Gitterpotential verursachen, an denen die Elektronen gestreut werden.
Amorphe Festkörper sind thermodynamisch metastabil. Der Nicht-Gleichgewichtszustand wird bei der Herstellung z.B. durch die Amorphisierung dünner Schichten oder durch verschiedene Abschreckmethoden bewusst hervorgerufen. Beim Erwärmen kristallisieren amorphe Substanzen in die stabilen kristallinen Phasen bei Temperaturen, die für metallische Legierungen typischerweise einige 100 K über Raumtemperatur liegen. [TV]
amorphe Festkörper: Schema der atomaren Anordnung in einem Kristall und in einem amorphen Festkörper (oben). Die entsprechenden radialen Verteilungsfunktionen r(r) geben die Wahrscheinlichkeit an, im Abstand r von einem Atom ein weiteres zu finden (unten).
Techniklexikon.net
Das freie Technik-Lexikon. Fundierte Informationen zu allen Fachgebieten der Ingenieurwissenschaften, für Wissenschaftler, Studenten, Praktiker & alle Interessierten. Professionell dargeboten und kostenlos zugängig.
Techniklexikon
Modernes Studium der Physik sollte allen zugängig gemacht werden.