Raoultsches Gesetz

Irene Kramer-Schwenk
Chemie,
Physikalische Chemie, gibt den Partialdruck der Komponenten einer flüssigen
Mischung in der koexistierenden Gasphase wieder. Bei einer idealen Lösung ist
der Dampfdruck pA einer Komponente A proportional dem Dampfdruck
![]() der reinen Komponente
A und hängt vom Molenbruch xA in der flüssigen Phase
ab:
der reinen Komponente
A und hängt vom Molenbruch xA in der flüssigen Phase
ab: ![]() .
.
In realen Lösungen sind die zwischenmolekularen Wechselwirkungen unterschiedlich. Das Raoultsche Gesetz ist in diesem Fall für das Lösungsmittel verdünnter Lösungen anwendbar, da dieses als Überschusskomponente in fast reiner Form vorliegt. Gehorcht das Verhalten der Unterschusskomponente zusätzlich dem Henryschen Gesetz, dann liegt eine ideal verdünnte Lösung vor.
Aus dem Raoultschen Gesetz folgt, dass die relative Dampfdruckerniedrigung, bzw. Siedepunktserhöhung von A in einer binären Lösung vom Molenbruch xB des gelösten Stoffes abhängt. Dies wird in der Ebullioskopie genutzt, um die Molmasse des gelösten Stoffes B zu bestimmen.
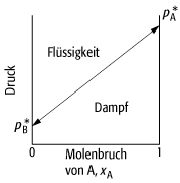
Raoultsches Gesetz: Das Dampfdruck-Diagramm einer binären Mischung zeigt die lineare Abhängigkeit des Gesamtdampfdrucks und der beiden partiellen Dampfdrücke von den Molenbrüchen der Komponenten.
Techniklexikon.net
Das freie Technik-Lexikon. Fundierte Informationen zu allen Fachgebieten der Ingenieurwissenschaften, für Wissenschaftler, Studenten, Praktiker & alle Interessierten. Professionell dargeboten und kostenlos zugängig.
Techniklexikon
Modernes Studium der Physik sollte allen zugängig gemacht werden.