Spektren mehratomiger Moleküle

Karl-Wilhelm Steinfieber
Atom- und Molekülphysik, Molekülspektren, die sich vom fernen Ultrarot bis zum ultravioletten Spektralbereich erstrecken und ähnlich wie die Spektren zweiatomiger Moleküle durch Kombination von Rotations-, Schwingungs- und Elektronenübergängen entstehen. Wegen der z.T. beträchtlichen Wechselwirkungsanteile ist die sich daraus ergebende Einteilung in Rotations-, Schwingungs-, Rotationsschwingungs- und Elektronenspektren aber ungenauer als bei den zweiatomigen Molekülen.
1) Rotationsspektren sind von der Gestalt des untersuchten Moleküls abhängig. Infrarotaktiv sind beispielsweise nur solche linearen Moleküle, die auf Grund ihres permanenten elektrischen Dipolmoments nicht spiegelsymmetrisch sind (z.B. HCN, COS), und nur diejenigen symmetrischen Kreiselmoleküle, bei denen senkrecht zur Drehachse ein permanentes elektrisches Dipolmoment vorliegt. Bei Vorliegen von asymmetrischen Kreiselmolekülen (z.B. H2O, C2H4) sind Rotationsenergie und Spektrum nicht mehr in geschlossener Form darstellbar.
2) Schwingungsspektren mehratomiger Moleküle enthalten für bestimmte Atomgruppierungen charakteristische Banden, die tabelliert sind und zur Strukturaufklärung von Molekülen genutzt werden können. Die Zahl der möglichen Normal- und Eigenschwingungen (siehe Abb. 1) eines Moleküls entspricht genau der Anzahl der Schwingungsfreiheitsgrade. Die Schwingungsformen werden in Valenz- und Deformationsschwingungen unterteilt (siehe Abb. 2). Die Schwingungsfrequenzen sind durch die Bindungskräfte zwischen den einzelnen Atomen festgelgt. Die Ermittlung dieser Bindungskräfte, die durch die Kraftkonstanten charakterisiert werden, ist eine der Hauptanliegen der Infrarot-Spektroskopie und der Raman-Spektroskopie.
3) Rotationsschwingungsspektren mehratomiger Moleküle sind relativ kompliziert, insbesondere kommt es durch die mit der Rotation verbundenen Coriolis-Kräfte zu einer Kopplung einzelner Normalschwingungen (Coriolis-Effekt), was dazu führen kann, dass die Atome in elliptischen Bahnen schwingen. Es tritt dann ein Schwingungsdrehimpuls mit der Quantenzahl l auf. Liegen zwischenmolekulare Wechselwirkungen, wie z.B. bei realen Gasen, vor, so kommt es zu einer Verbreiterung der einzelnen Rotationslinien. Im flüssigen Zustand fehlt die Rotationsstruktur der Spektrallinien. Dagegen wird die Schwingungsstruktur vom Aggregatzustand nur geringfügig beeinflusst. Beim Übergang vom Gas zur Flüssigkeit können durch die Bildung von Molekülaggregaten, z.B. Wasserstoffbrückenbindungen, neue Banden auftreten.
4) Elektronenspektren mehratomiger Moleküle enthalten Elektronenbanden, die analog zu denjenigen zweiatomiger Moleküle durch kombinierte Elektronenschwingungs- und Rotationsübergänge, ausgehend vom Elektronengrundzustand des Moleküls, entstehen (Elektronenschwingungsspektrum).
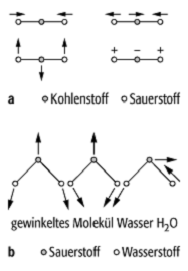
Spektren mehratomiger Moleküle 1: Normalschwingungen a) eines linearen (CO2) und b) eines gewinkelten (H2O) XY2-Moleküls.
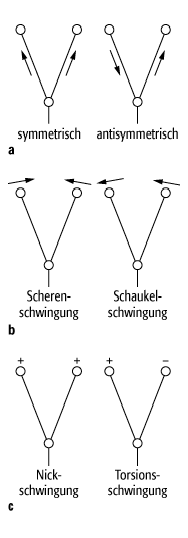
Spektren mehratomiger Moleküle 2: Mögliche Schwingungsformen: a) Valenzschwingungen, b) Deformationsschwingungen in der Ebene, c) Deformationsschwingungen aus der Ebene heraus.
Techniklexikon.net
Das freie Technik-Lexikon. Fundierte Informationen zu allen Fachgebieten der Ingenieurwissenschaften, für Wissenschaftler, Studenten, Praktiker & alle Interessierten. Professionell dargeboten und kostenlos zugängig.
Techniklexikon
Modernes Studium der Physik sollte allen zugängig gemacht werden.