Elektronegativität

Martina Wagner
Chemie, Physikalische Chemie, EN, c, »Mass für die Stärke eines Atoms in einem Molekül, Elektronen an sich zu ziehen« (L. Pauling, 1932). Sie ist keine Eigenschaft des isolierten Atoms, sondern des Atoms in seiner Umgebung. Paulings Elektronegativitätsskala, die auf thermodynamischen Daten (Energie der Valenzelektronen) beruht, ist willkürlich so gewählt, dass Wasserstoff den Wert 2,1 und das elektronegativste Element Fluor den Wert 4 besitzt. R.S. Mulliken hat eine Skala mit absoluten Einheiten abgeleitet und berechnet. Seine Definition für die Elektronegativität lautet:
![]() ,
,
wobei die Ionisierungsenergie IEV und die Elektronenaffinität EAV des Valenzzustands in eV eingesetzt werden. Die Mulliken-Werte können mit folgender Gleichung in die Werte von Pauling umgerechnet werden:
![]() .
.
Die Definition der Elektronegativität nach Mulliken ist gleich dem Anstieg der Energiekurve der Ionisierungsenergie und der Elektronenaffinität (in Abhängigkeit von der Oxidationsstufe) im Ursprung (z = 0):
![]() .
.
Ein hoher Anstieg der Energiekurve z.B. bedeutet, dass bei der Aufnahme eines Elektrons viel Energie frei wird und das entsprechende Atom sehr elektronegativ sein wird. Es besteht auch ein Zusammenhang zwischen EN und der Säure-Base-Eigenschaft eines Moleküls.
L.C. Allen definierte die Elektronegativität eines Atoms mittels Orbitalenergien und bezeichnete sie als dessen Konfigurationsenergie CE:
![]() .
.
Hierbei sind m und n die Anzahl bzw. ep und es die Energien der Elektronen in den p- und s-Orbitalen der Valenzschale. Sie lassen sich spektroskopisch bestimmen. Die CE kann die periodischen Eigenschaften der Elemente wie z.B. die kovalente, ionische und metallische Bindung, die Atomradien und Oxidationszahlen, sowie die besonderen Eigenschaften von Kohlenstoff und Wasserstoff beschreiben.
Die Elektronegativität eines Atoms ist nicht unveränderlich, sondern hängt von seinem Valenzzustand (Hybridisierung) und von der Ladung ab.
Die Elektronegativität der Elemente unterliegt einer Periodizität. Innerhalb einer Periode des Periodensystems nehmen die Elektronegativitäten mit steigender Ordnungszahl n zu. Dagegen nehmen die EN innerhalb einer Gruppe von oben nach unten ab.
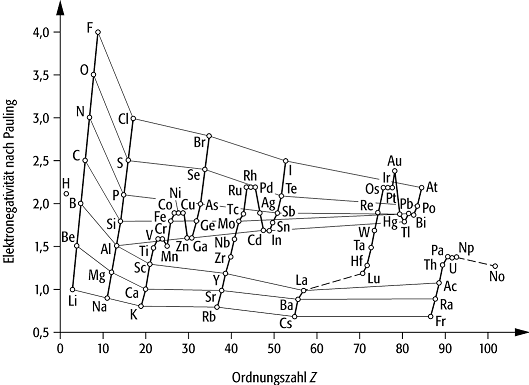
Elektronegativität: Änderung der Elektronegativität der Elemente in Abhängigkeit von der Ordnungszahl (Periodizität).
Techniklexikon.net
Das freie Technik-Lexikon. Fundierte Informationen zu allen Fachgebieten der Ingenieurwissenschaften, für Wissenschaftler, Studenten, Praktiker & alle Interessierten. Professionell dargeboten und kostenlos zugängig.
Techniklexikon
Modernes Studium der Physik sollte allen zugängig gemacht werden.