Enzyme

Martina Wagner
Biophysik, Fermente, Biomakromoleküle, die als Biokatalysatoren an den chemischen Umwandlungen unter den Bedingungen lebender Systeme in vivo beteiligt sind. Ihre Funktion besteht in der Verringerung der Aktivierungsenergie und damit in der Beschleunigung chemischer Reaktionen. Viele Enzyme haben eine enorme katalytische Leistung, verglichen mit Katalysatoren abiogenen Ursprungs. Sie ermöglichen bei niedrigen Temperaturen, normalem atmosphärischen Druck und geringen Konzentrationen den Ablauf von chemischen Reaktionen, welche bei Abwesenheit des Biokatalysators nur unter extremen Reaktionsbedingungen eintreten würden. Ein klassisches Beispiel ist Umwandlung von Luftstickstoff (N2) zu Ammoniak (NH3) im Haber-Bosch-Verfahren (Temperatur von 250 oC und Druck von ca. 300 atm!) und durch N2-fixierende Bakterien (frei lebend oder in Symbiose z.B. in Wurzelknöllchen von Sojabohnen, Temperatur von 20 oC und 1 atm). Durch das Hintereinanderschalten mehrerer enzym-katalysierter Reaktionen eines Substrates S zu einem Produkt P wie in entstehen Fliessgleichgewichte, mit deren Hilfe es biologischen Systemen gelingt, auch thermodynamisch ungünstig liegende Reaktionen nahezu vollständig in der erforderlichen Richtung ablaufen zu lassen.
Enzymanwendungen sind ein wichtiger Teil der Biotechnologie. In der medizinischen Diagnostik spielen Aktivitätsbestimmungen von Enzymen im Blutserum oder Harn eine grosse Rolle.Chemische Struktur: Die überaus grösste Zahl der bekannten Enzyme sind Proteine, aber seit den achziger Jahren sind auch eine Reihe von Ribozymen (Biokatalysatoren auf der Basis von RNS) bekannt. Oft sind Enzyme Proteide (zusammengesetzte Proteine). Wirkungsmechanismus: Auf dem Wege des Überganges vom Substrat zum Produkt entlang der sogenannten Reaktionskoordinate überwindet die enzymatische Reaktion eine Energiebarriere (Abb. 2). Ihre Höhe ist die Aktivierungsenergie EA. Man geht davon aus, dass der erste Schritt der enzymatischen Reaktion die Bildung eines »aktivierten Komplexes« ist. Das Substrat geht dabei nichtkovalente Wechselwirkungen, Wasserstoffbrücken und eventuell auch kovalente Bindungen mit dem aktiven Zentrum ein (Enzym-Substrat-Komplex). Durch das Enzym wird dabei die Elektronenverteilung im Substrat in der Weise geändert, dass der sogenannte Übergangszustand (transition state) stabilisiert wird. Er ist der Zustand mit der höchsten Energie auf dem Weg vom Substrat zum Produkt. Die Stoffumwandlungsprozesse bei der enzymatischen Katalyse bedürfen quantenchemischer Beschreibung. (enzymatische Katalyse) [FE]
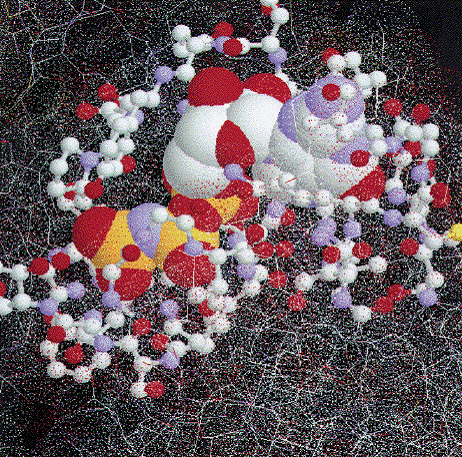
Enzyme 1: Bindung von Guanosin-5¢-Triphosphorsäure (GTP) durch das H-Ras-P21-Onkogen-Protein (Enzym aus einer zellulären Signaltransduktionskaskade, Eintrag 521P der Brookhaven Protein Data Bank). Das vollständige (hier chemisch modifizierte) GTP ist als CPK-Modell dargestellt. Die Van-der-Waals-Oberfläche des nur teilweise gezeigten Proteins ist mit einem feinen Punktnetz angedeutet, um Einsicht in die Bindungstasche zu ermöglichen. Während die Polypeptidkette generell als Drahtmodell gezeigt wird, sind alle Aminosäuren in unmittelbarer Nähe des GTP als Ball-Balken-Modell dargestellt worden. Die Farben Weiss, Rot, Blau und Gelb kodieren die Elemente Kohlenstoff, Sauerstoff, Stickstoff und Phosphor.
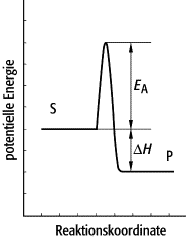
Enzyme 2: Energetische Reaktionskurve. Die Reaktionskoordinate (die Abszisse) beschreibt auf geeignete Weise die gegenseitige Lage der an der Reaktion beteiligten Partnermoleküle. Auf der Ordinate ist die potentielle Energie abgetragen. Der Weg vom Substrat zum Produkt wird durch eine energetische Barriere mit der Höhe der Aktivierungsenergie EA versperrt.
Techniklexikon.net
Das freie Technik-Lexikon. Fundierte Informationen zu allen Fachgebieten der Ingenieurwissenschaften, für Wissenschaftler, Studenten, Praktiker & alle Interessierten. Professionell dargeboten und kostenlos zugängig.
Techniklexikon
Modernes Studium der Physik sollte allen zugängig gemacht werden.