Isotope

Julian Schultheiss
Aus dem griech. »isos« gleich und »topos« - Platz abgeleiteter Begriff für Nuklide ein und desselben Elements, die im »Periodensystem der Elemente« an gleicher Stelle stehen, sich aber durch die Anzahl der Neutronen im Atomkern (Atom) voneinander unterscheiden. I. sind praktisch Modifikationen eines ehem. Elements. Die nichtstabilen I. bezeichnet man als »Radioisotope« oder »Radionuklide«. I. entstehen sowohl auf natürliche Weise als auch durch künstlich herbeigeführte Kernreaktionen.
Nuklide, deren Kerne
gleich viele Protonen, aber unterschiedlich viele Neutronen enthalten und
deswegen verschiedene Massen haben. Ein bekanntes Beispiel sind die drei
Isotope des natürlichen Wasserstoffs ![]() , die im Falle
des 1H aus
einem Proton, im Fall des Deuterium 2D aus einem Proton und einem Neutron und im
Fall von Tritium 3T
aus einem Proton und zwei Neutronen bestehen. Wegen der stets gleichen
Protonenzahl, d.h. gleichen Kernladungszahl, haben die Isotope auch die gleiche
Anzahl von Elektronen in der Hülle und gehören somit zum gleichen chemischen
Element. Ausser in der Masse unterscheiden sich Isotope noch im Kernvolumen, in
der Spinquantenzahl und magnetischen Quantenzahl des Atomkerns, die Isotope der
leichtesten Elemente auch geringfügig im chemischen Verhalten.
, die im Falle
des 1H aus
einem Proton, im Fall des Deuterium 2D aus einem Proton und einem Neutron und im
Fall von Tritium 3T
aus einem Proton und zwei Neutronen bestehen. Wegen der stets gleichen
Protonenzahl, d.h. gleichen Kernladungszahl, haben die Isotope auch die gleiche
Anzahl von Elektronen in der Hülle und gehören somit zum gleichen chemischen
Element. Ausser in der Masse unterscheiden sich Isotope noch im Kernvolumen, in
der Spinquantenzahl und magnetischen Quantenzahl des Atomkerns, die Isotope der
leichtesten Elemente auch geringfügig im chemischen Verhalten.
Man unterscheidet zwischen stabilen und radioaktiven Isotopen
(Radionukliden), die unter Aussendung von ionisierender Strahlung zerfallen,
wie im obigen Beispiel das Tritium 3T. Nur etwa 20 chemische Elemente bestehen
aus einem einzigen Isotop. Beispiele hierfür sind ![]() . Die übrigen
Elemente sind eine Mischung von Isotopen, die mit verschiedenen Häufigkeiten in
der Mischung enthalten sind, z.B.
. Die übrigen
Elemente sind eine Mischung von Isotopen, die mit verschiedenen Häufigkeiten in
der Mischung enthalten sind, z.B.
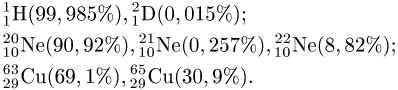
Bekannt sind heute knapp 300 stabile und über 2400 instabile Isotope. Jedes Element besitzt mindestens drei Isotope. Am meisten stabile Isotope hat Zinn. Am meisten Isotope überhaupt sind beim Xenon bekannt. Die Elemente mit Ordnungszahlen über 83 haben nur noch radioaktive Isotope.
Untersuchungen ergaben, dass Mischelemente, die aus mehreren Isotopen zusammengesetzt sind, sowohl auf der Erde als auch in Meteoriten fast stets das gleiche Mischungsverhältnis der einzelnen Isotope aufweisen. Die sicherste Unterscheidung der Isotope, die auch gleichzeitig ihre Massen zu messen gestattet, gelingt mit einem Massenspektrographen. Ebenso gibt es eine grössere Anzahl von Methoden zur Isotopentrennung in technischem Ausmass, so dass man über viele Isotope in reinem Zustand verfügt. Radioaktive Isotope können für spezielle Anwendungszwecke künstlich hergestellt werden (künstliche Radioaktivität).
Die Verwendung der stabilen Isotopen erstreckt sich auf die Gebiete der Chemie, Physik, Biologie, Medizin. Man setzt sie dort zur Markierung von zu untersuchenden Stoffen ein. In grossem Umfang wird Deuteriumoxid als wirksame Bremssubstanz für Neutronen in Kernreaktoren eingesetzt; das gasförmige Bortrifluorid 10BF3 mit dem seltenen Borisotop 10B dient zur Füllung von Neutronenzählern ähnlich wie das Isotop 3He. Radionuklide sind zur Untersuchung elementarer Lebensprozese auf der Ebene molekularer Organisationen in bestimmten Organen und Geweben eines Patienten heute unentbehrliches Werkzeug der medizinischen Diagnostik. Darüber hinaus können sie auch therapeutisch höchst wirksam sein.
In der Klimatologie sind Isotopenmessungen ein wichtiges Hilfsmittel zur Rekonstruktion von Klimaänderungen in der Vergangenheit.
Techniklexikon.net
Das freie Technik-Lexikon. Fundierte Informationen zu allen Fachgebieten der Ingenieurwissenschaften, für Wissenschaftler, Studenten, Praktiker & alle Interessierten. Professionell dargeboten und kostenlos zugängig.
Techniklexikon
Modernes Studium der Physik sollte allen zugängig gemacht werden.