Dampf

Hermann Loring
gasförmige Phase eines Stoffes, der entweder in Wechselwirkung mit seiner flüssigen oder festen Phase steht oder der sich in einem Zustand befindet, aus dem er durch kleine Temperatur- oder Druckänderungen zur Kondensation gebracht werden kann.
Meist entsteht Dampf durch Verdampfung (Sieden) bzw. Sublimation, d.h. durch Austritt von Molekülen aus der Oberfläche der flüssigen bzw. festen Phase in die dampf- oder gasförmige Phase. Zwischen der Flüssigkeit bzw. dem festen Körper und ihrem Dampf stellt sich ein Gleichgewicht ein, das nur von der Temperatur abhängt und durch einen bestimmten Dampfdruck charakterisiert ist. Alle drei Aggregatzustände, fest, flüssig und gasförmig, stehen am Tripelpunkt im Gleichgewicht. Der Zusammenhang zwischen einer Flüssigkeit und ihrem Dampf lässt sich im p,V-Diagramm gut erkennen. Komprimiert man ein Gas entlang einer Isotherme (z.B. bei A beginnend), so erreicht man bei B eine obere Grenzkurve. Von B aus ist zunächst keine weitere Drucksteigerung durch Volumenverminderung möglich. Unter Nebelbildung tritt Verflüssigung ein, und es entsteht eine Flüssigkeitsoberfläche. An der unteren Grenzkurve bei C ist alles flüssig. Unter starker Drucksteigerung ist weitere Volumenverminderung möglich (D). Oberhalb der kritischen Isotherme lässt sich das Gas isotherm nicht verflüssigen. Der Dampf im Zweiphasengebiet (zwischen oberer und unterer Grenzkurve) ist gesättigter Dampf, der technisch als Nassdampf bezeichnet wird, und der ebenfalls gesättigte Dampf auf der oberen Grenzkurve heisst Sattdampf, Trockendampf oder trockengesättigter Dampf, der ungesättigte Dampf rechts der oberen Grenzkurve überhitzter Dampf oder Heissdampf.
Für die Dichte einer Flüssigkeit rF und ihres Dampfes rD gilt die Cailletet-Matthiassche Regel, wonach der Mittelwert der Dichten eine lineare Funktion der absoluten Temperatur T ist:
![]()
Dabei sind a und b Stoffkonstanten. Aus der Cailletet-Matthiasschen Regel lässt sich bei bekannter kritischer Temperatur Tc die kritische Dichte berechnen. Der Dampf über flüssigen Mischungen setzt sich im allgemeinen aus dem Dampf der Komponenten der Mischung zusammen, wobei die Komponente mit höherem Dampfdruck im Dampf angereichert ist.
Der in Natur und Technik wichtigste Dampf ist der Wasserdampf.
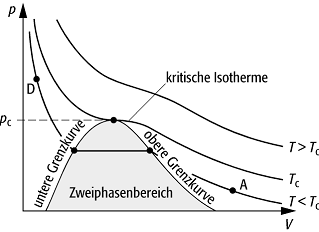
Dampf: p,V-Diagramm eines aus einer Flüssigkeit und ihrem Dampf bestehenden Systems.
Techniklexikon.net
Das freie Technik-Lexikon. Fundierte Informationen zu allen Fachgebieten der Ingenieurwissenschaften, für Wissenschaftler, Studenten, Praktiker & alle Interessierten. Professionell dargeboten und kostenlos zugängig.
Techniklexikon
Modernes Studium der Physik sollte allen zugängig gemacht werden.