Boltzmann-Verteilung

Martina Wagner
im engeren Sinne die Energieverteilung der Gasteilchen in einem klassischen idealen Gas, das sich im thermodynamischen Gleichgewicht befindet, in einem weiteren Sinne die Besetzungsverteilung eines physikalischen Systems im thermischen Gleichgewicht. Die Boltzmann-Verteilung für ein ideales Gas folgt unmittelbar aus der kanonischen Verteilung, wenn man sich vorstellt, dass für jedes Gasteilchen alle übrigen Gasteilchen ein Wärmebad bilden. Der Anteil n(E)dE der Teilchen mit einer Energie zwischen E und E + dE ist dann
![]() ,
,
wobei kB die Boltzmann-Konstante, T die absolute Temperatur,
g(E)dE die Zustandsdichte bei der Energie E und C
eine Normierungskonstante ist, die sich aus der Bedingung 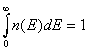 ergibt. Für freie Gasteilchen ist E die
kinetische Energie Ekin
= m
ergibt. Für freie Gasteilchen ist E die
kinetische Energie Ekin
= m![]() 2/2, und man erhält mit g(E)dE
~
2/2, und man erhält mit g(E)dE
~
![]() 2d
2d![]() ~ E1/2dE die
Maxwellsche Geschwindigkeitsverteilung. Verwendet man die potentielle Energie
im homogenen Schwerefeld Epot = mgh, ergibt sich die barometrische Höhenformel.
Die Boltzmann-Verteilung gilt stenggenommen nur für klassische ideale Gase,
d.h. für Gase,
~ E1/2dE die
Maxwellsche Geschwindigkeitsverteilung. Verwendet man die potentielle Energie
im homogenen Schwerefeld Epot = mgh, ergibt sich die barometrische Höhenformel.
Die Boltzmann-Verteilung gilt stenggenommen nur für klassische ideale Gase,
d.h. für Gase,
a) die mit der klassischen Maxwell-Boltzmann-Statistik statt mit der Quantenstatistik (Bose-Einstein, Fermi-Dirac) beschrieben werden können und
b) bei denen es keine Wechselwirkung zwischen den Gasteilchen gibt.
Im Bereich mit E >> kBT, dem "hochenergetischen Schwanz", stellt sie allerdings auch für die quantenstatistischen Verteilungen sowie für reale Gase und Lösungen ein gute Näherung dar. Da man häufig am Anteil der Teilchen oberhalb einer bestimmten, hohen Energie interessiert ist - physikalische Effekte werden am ehesten von Teilchen hoher Energie bewirkt - hat die Boltzmann-Verteilung praktisch universelle Gültigkeit. So haben die Richardson-Gleichung für den Glühemissionsstrom als Funktion der Temperatur - hier ist für E die Austrittsarbeit einzusetzen - und das Wiensche Strahlungsgesetz als Grenzfall des Planckschen Strahlungsgesetzes für hn >> kBT beide die Form y = C exp ( - E/kBT), obwohl streng genommen im ersten Fall das Elektronengas nach der Fermi-Dirac-Statistik und im zweiten Fall das Photonengas nach der Bose-Einstein-Statistik beschrieben werden muss. Bei chemischen Reaktionen erhält man, wenn man für E die Aktivierungsenergie einsetzt, das Arrhenius-Gesetz für die Temperaturabhängigkeit der Reaktionsgeschwindigkeit. Die Temperaturabhängigkeit der Gleichgewichtskonstante kann man dagegen berechnen, wenn man für E die Reaktionsenthalpie verwendet.
Bei einem quantenmechanischen System mit mehreren möglichen diskreten Energiezuständen Ei , das der klassischen Statistik gehorcht, ist die Wahrscheinlichkeit, es im Zustand mit der Energie Ei zu finden, gegeben durch:
![]() ,
,
wobei gi die statistischen Gewichte der einzelnen Zustände sind. Durch sie wird berücksichtigt, dass verschiedene Zustände auch bei gleicher Energie unterschiedliche Wahrscheinlichkeiten haben können. a ist ein Normierungsfaktor, der berücksichtigt, dass die Summe über die Besetzungswahrscheinlichkeiten aller Zustände 1 ergeben muss. Die Boltzmann-Verteilung beschreibt dann z.B. die Verteilung von Atomen und Molekülen auf die möglichen Eigenzustände. In diesem Fall wäre das statistische Gewicht die Anzahl der entarteten Unterzustände des betreffenden Zustands, normiert auf die Gesamtzahl von Unterzuständen des Systems.
Techniklexikon.net
Das freie Technik-Lexikon. Fundierte Informationen zu allen Fachgebieten der Ingenieurwissenschaften, für Wissenschaftler, Studenten, Praktiker & alle Interessierten. Professionell dargeboten und kostenlos zugängig.
Techniklexikon
Modernes Studium der Physik sollte allen zugängig gemacht werden.